lunes, 28 de mayo de 2012
| El Efecto Doppler en la Física Clásica y en la Física Relativista | |||||||||||||||||||
| la sirena de la ambulancia y el bicho en el estanque Todos hemos notado que la altura (una de las características de un sonido) de la sirena de una ambulancia que se aproxima se reduce bruscamente cuando la ambulancia pasa al lado nuestro  para alejarse. Esto es lo que se llama "Efecto Doppler". El
fenómeno fue descripto por primera vez por el matemático y físico austríaco Christian Doppler
(1803-1853). El cambio de altura se llama en Física "desplazamiento de la
frecuencia" de las ondas sonoras. Cuando la ambulancia se
acerca, las ondas provenientes de la
sirena se comprimen, es decir, el tamaño de las ondas disminuye, lo cual se traduce en
la percepción de una frecuencia o altura mayor.
Cuando la ambulancia se aleja, las ondas se separan en relación con el
observador causando que la frecuencia observada sea menor que la de la
fuente. Por el cambio
en la altura de la sirena, se puede saber si la misma se está alejando o
acercando. Si se pudiera medir la velocidad de cambio de la altura, se
podría también estimar la velocidad de la ambulancia.
para alejarse. Esto es lo que se llama "Efecto Doppler". El
fenómeno fue descripto por primera vez por el matemático y físico austríaco Christian Doppler
(1803-1853). El cambio de altura se llama en Física "desplazamiento de la
frecuencia" de las ondas sonoras. Cuando la ambulancia se
acerca, las ondas provenientes de la
sirena se comprimen, es decir, el tamaño de las ondas disminuye, lo cual se traduce en
la percepción de una frecuencia o altura mayor.
Cuando la ambulancia se aleja, las ondas se separan en relación con el
observador causando que la frecuencia observada sea menor que la de la
fuente. Por el cambio
en la altura de la sirena, se puede saber si la misma se está alejando o
acercando. Si se pudiera medir la velocidad de cambio de la altura, se
podría también estimar la velocidad de la ambulancia.Una fuente emisora de ondas sonoras que se aproxima, se acerca al observador durante el período de la onda. Y, dado la longituda de la onda se acorta y la velocidad de propagación de la onda permanece sin cambios, el sonido se percibe más alto. Por esta misma razón, la altura de una fuente que se aleja, se reduce. El Efecto Doppler se observa en ondas de todo tipo (ondas sonoras, ondas electromagnéticas, etc.). Consideremos el caso de las ondas en la superficie del agua: supongamos que en el centro de  un estanque hay un bicho moviendo
sus patas periódicamente. Si las ondas se originan en un punto, se moverán desde ese punto en todas direcciones. Como cada
perturbación viaja por el mismo medio, todas las ondas viajarán a la misma
velocidad y el patrón producido por el movimiento
del bicho sería un conjunto de círculos concéntricos como se muestra en
la figura. Estos círculos alcanzarán los bordes del estanque a la misma
velocidad. Un observador en el punto A (a la izquierda) observaría la
llegada de las perturbaciones con la misma frecuencia que otro B (a la
derecha). De hecho, la frecuencia a la cual las perturbaciones llegarían
al borde sería la misma que la frecuencia a la cual el bicho las produce. Si el bicho produjera,
por ejemplo, 2 perturbaciones por segundo,
entonces cada observador detectaría 2 perturbaciones por segundo. un estanque hay un bicho moviendo
sus patas periódicamente. Si las ondas se originan en un punto, se moverán desde ese punto en todas direcciones. Como cada
perturbación viaja por el mismo medio, todas las ondas viajarán a la misma
velocidad y el patrón producido por el movimiento
del bicho sería un conjunto de círculos concéntricos como se muestra en
la figura. Estos círculos alcanzarán los bordes del estanque a la misma
velocidad. Un observador en el punto A (a la izquierda) observaría la
llegada de las perturbaciones con la misma frecuencia que otro B (a la
derecha). De hecho, la frecuencia a la cual las perturbaciones llegarían
al borde sería la misma que la frecuencia a la cual el bicho las produce. Si el bicho produjera,
por ejemplo, 2 perturbaciones por segundo,
entonces cada observador detectaría 2 perturbaciones por segundo.Ahora supongamos que el bicho estuviera moviéndose hacia la derecha a lo largo del estanque produciendo también 2 perturbaciones por segundo. Dado que el bicho se desplaza hacia la  derecha, cada perturbación se origina en una posición
más cercana a B y más lejana a A. En consecuencia, cada perturbación
deberá recorrer una distancia menor para llegar a B y tardará menos en
hacerlo. Por lo tanto, el observador B registrará una frecuencia de llegada de
las perturbaciones mayor que la frecuencia a la cual son producidas. Por
otro lado, cada perturbación deberá recorrer una distancia mayor para
alcanzar el punto A. Por esta razón, el observador A registrará una
frecuencia menor. El efecto neto del movimiento del bicho (fuente de las
ondas) es que el observador hacia el cual se dirige observe una
frecuencia mayor que 2 por segundo y el observador del cual se aleja
perciba una frecuencia menor que 2 por segundo. derecha, cada perturbación se origina en una posición
más cercana a B y más lejana a A. En consecuencia, cada perturbación
deberá recorrer una distancia menor para llegar a B y tardará menos en
hacerlo. Por lo tanto, el observador B registrará una frecuencia de llegada de
las perturbaciones mayor que la frecuencia a la cual son producidas. Por
otro lado, cada perturbación deberá recorrer una distancia mayor para
alcanzar el punto A. Por esta razón, el observador A registrará una
frecuencia menor. El efecto neto del movimiento del bicho (fuente de las
ondas) es que el observador hacia el cual se dirige observe una
frecuencia mayor que 2 por segundo y el observador del cual se aleja
perciba una frecuencia menor que 2 por segundo.El Efecto Doppler se observa siempre que la fuente de ondas se mueve con respecto al observador. Es el efecto producido por una fuente de ondas móvil por el cual hay un aparente desplazamiento de la frecuencia hacia arriba para los observadores hacia los cuales se dirige la fuente y un aparente desplazamiento hacia abajo de la frecuencia para los observadores de los cuales la fuente se aleja. Es importante notar que el efecto no se debe a un cambio real de la frecuencia de la fuente. En el ejemplo anterior, el bicho produce en los dos casos 2 perturbaciones por segundo; sólo aparentemente para el observador al cual el bicho se acerca parece mayor.El efecto se debe a que la distancia entre B y el bicho se reduce y la distancia a A aumenta. El Efecto Doppler en Astronomía Como se ha señalado más arriba, en el caso de la radiación electromagnética emitida por un objeto en movimiento también se presenta el Efecto Doppler. La radiación emitida por un objeto que se mueve hacia un observador se comprime; su frecuencia se percibe aumentada y se dice que la frecuencia "se desplaza hacia el azul". Por el contrario, la radiación emitida por un objeto que se aleja se estira, "se desplaza hacia el rojo". Los desplazamientos hacia el azul o hacia el rojo que exhiben las estrellas, galaxias y nebulosas indican su movimiento con respecto a la Tierra. En Astronomía, el Efecto Doppler fue estudiado originalmente en la parte visible del espectro electromagnético. Hoy, el "desplazamiento Doppler", como también se lo conoce, se estudia en todo el espectro de ondas. Debido a la relación inversa que existe entre frecuencia y longitud de onda, podemos describir el desplazamiento Doppler en términos de longitudes de onda. La radiación se corre hacia el rojo cuando la longitud de onda aumenta y se corre hacia el azul cuando la longitud de onda disminuye. Los astrónomos se basan en el desplazamiento Doppler para calcular con precisión la velocidad de las estrellas y otros cuerpos celestes con respecto a la Tierra y para determinar si se acercan o se alejan. Por ejemplo, las líneas espectrales del gas hidrógeno en galaxias lejanas es frecuentemente observada con un corrimiento hacia el rojo considerable. La línea del espectro de emisión, que normalmente (en la Tierra) se encuentra en una longitud de onda de 21 centímetros, puede ser observada a 21,1 centímetros. Este milímetro de corrimiento hacia el rojo indicaría que el gas se está alejando de la Tierra a 1400 kilómetros por segundo. Más aún, estudiando el Efecto Doppler, se puede obtener información acerca de estrellas específicas. Las galaxias son grupos de estrellas que en general rotan alrededor de su centro de masa. La radiación electromagnética emitida por cada estrella de una galaxia distante aparecerá desplazada hacia el rojo si la estrella al rotar se aleja de la Tierra. En el caso contrario aparecerá desplazada hacia el azul. Pero debe tomarse en cuenta lo siguiente: Los desplazamientos de frecuencia pueden ser el resultado de otros fenómenos, no del movimiento relativo del observador y la fuente. Otros dos fenómenos pueden estar involucrados: la existencia de campos gravitacionales muy fuertes que dan origen al "desplazamiento gravitacional hacia el rojo"; y el llamado "desplazamiento cosmológico hacia el rojo", debido a la expansión del espacio producto de la Gran Explosión. Fórmulas y cálculos Para poder expresar con números el fenómeno descripto en la sección anterior, consideremos los esquemas siguientes:
El cálculo de estas longitudes de onda a partir de la velocidad de propagación de la onda, la velocidad de la fuente (F) y el período se hace con las siguientes fórmulas:
El
siguiente formulario permite calcular las frecuencias de ondas sonoras percibidas por
causa del Efecto Doppler.
|
SOLUBILIDAD
Otra propiedad física que permite conocer el tipo de enlace es la solubilidad. Los compuestos con enlace iónico son solubles en agua y los que tienen enlace covalente se disuelven en otros compuestos covalentes. Esta propiedad tiene varias excepciones, la fundamental es que las sustancias que tienen moléculas con muchos átomos de oxígeno y que no son macromoléculas son solubles en agua porque los átomos de oxígeno se unen con los átomos de hidrógeno del agua.
Prácticamente todos los compuestos formados con elementos situados a la derecha de la tabla periódica tienen enlaces covalentes. En la vida corriente serían todas las pinturas, disolventes, grasas, hidrocarburos, azúcar, alcohol, etc.
La solubilidad es la capacidad de una sustancia de disolver a otra, no necesariamente tienen que ser líquidas, pueden estar en los tres estados de la materia, por ejemplo las gaseosas son gases disueltos en líquidos, el talco es un sólido que absorbe líquidos. Hay factores que intervienen aumentando o disminuyendo esta capacidad, la presión es el menos importante, otros tienen mas trascendencia como:
Otra propiedad física que permite conocer el tipo de enlace es la solubilidad. Los compuestos con enlace iónico son solubles en agua y los que tienen enlace covalente se disuelven en otros compuestos covalentes. Esta propiedad tiene varias excepciones, la fundamental es que las sustancias que tienen moléculas con muchos átomos de oxígeno y que no son macromoléculas son solubles en agua porque los átomos de oxígeno se unen con los átomos de hidrógeno del agua.
Prácticamente todos los compuestos formados con elementos situados a la derecha de la tabla periódica tienen enlaces covalentes. En la vida corriente serían todas las pinturas, disolventes, grasas, hidrocarburos, azúcar, alcohol, etc.
La solubilidad es la capacidad de una sustancia de disolver a otra, no necesariamente tienen que ser líquidas, pueden estar en los tres estados de la materia, por ejemplo las gaseosas son gases disueltos en líquidos, el talco es un sólido que absorbe líquidos. Hay factores que intervienen aumentando o disminuyendo esta capacidad, la presión es el menos importante, otros tienen mas trascendencia como:
- Afinidad entre las dos sustancias
- Concentración del soluto
- Tipos de enlace
- Grado de división del soluto
- Temperatura.
ENLACES QUIMICOS
ENLACES QUIMICOS
 ®
® 


 ®
® 



Solo los gases nobles se
presentan como átomos separados, en los materiales de nuestra vida diaria en su
mayoría los elementos están unidos por enlaces químicos .Un enlace químico es
representado por líneas entre átomos ó
palos conectando esferas, pero en términos químicos es el efecto que causan dos
átomos lo suficientemente cerca para estar a
mas baja energía que cuando ellos están a otra distancia y es del orden
de 100 kj por mol. Las fuerzas atractivas que mantienen juntos los elementos
que conforman un compuesto, se explican por la interacción de los electrones
que ocupan los orbitales más exteriores de ellos. Las propiedades periódicas
como la energía de ionización y la afinidad electrónica, predicen la
transferencia directa de electrones entre elementos y conformar enlaces de tipo
iónico ó compartir los electrones
de los niveles mas externos para conformar configuraciones más estables
(de gas noble)y formar enlaces de tipo
covalente. Las propiedades físicas y químicas para la gran mayoría de los
compuestos se explican por las diferencias que presentan los tipos de enlace
entre los elementos. El resultado de estas atracciones permite definir las moléculas como agregados de átomos con
propiedades distintas y distinguibles; de hecho las moléculas pueden ser muy
estables o altamente reactivas
El enlace iónico
Cuando se transfieren electrones de un elemento metálico a
uno no metálico, existe una atracción electrovalente entre el catión y el anión
lo cual produce un compuesto de tipo iónico y cuya estructura generalmente es
cristalina, como es el caso del sodio y la el cloro que por sus distribuciones
electrónicas buscan una mayor estabilidad formando una sal donde cada ión de
cloro esta rodeado por seis cationes de sodio y cada sodio rodeado por seis aniones de cloro.
Mediante una transferencia de un
electrón al cloro de cada sodio
adquiere la distribución del neón Na[Ne]3s1 ®Na+ [Ne]+ e-
Mediante la transferencia de un
electrón del sodio, el cloro adquiere la distribución del argón Cl[Ne]3s23p5
+ e- ®Cl-
[Ar]
 ®
® 

El enlace covalente
Cuando
no existe suficiente diferencia de electronegatividad para que exista transferencia electrónica, resultan dos átomos
compartiendo uno o más pares de electrones y forman una molécula con energía de
atracción débil en resultado poseen bajos puntos de fusión y ebullición en
comparación con los iónicos. Los enlaces pueden ser simple, doble y triple,
según la forma de compartir uno, dos o tres electrones.
La energía de las fuerzas de
atracción o repulsión entre los
elementos que conforman un enlace iónico es función de la distancia internuclear llegando a una distancia mínima
donde se compensa las fuerzas de
atracción y de repulsión, la cual se denomina distancia de enlace.

 ®
® 
La energía potencial de un sistemas de dos
átomos, presenta un comportamiento donde a grandes distancias no hay
interacción, a distancia de varios diámetros atómicos predomina la atracción y
distancias muy cercanas predomina la repulsión, causando que la energía
potencial aumente . Las energías de atracción y repulsión se equilibran en el
mínimo punto de la curva; a dicha distancia los átomos son estables y se dice
que el enlace químico existe entre ellos.
Las estructuras de Lewis.
Son formulas electrónicas propuestas por Gilbert Lewis en 1916 para los enlaces covalentes, se presenta en forma de puntos el números de electrones de los niveles de valencia o sea los electrones químicamente importantes, y en especial para los elementos del grupo A que tratan de tener la configuración de gas noble, como el cloro donde se predice la formación de un enlace covalente, en el oxigeno y azufre dos enlaces covalente, en el nitrógeno y fósforo se predicen tres en laces covalentes y en el carbono cuatro enlaces covalentes. Debido al gran numero de puntos esta representación no es muy útil en los elementos de transición. Para las formulas de Lewis todos los elementos de un mismo grupo tienen la misma configuración electrónica de los niveles más externos.
Como primera aproximación para la estructura de los enlaces
las formulas de Lewis y solo muestra los, electrones de valencia y además, no
permite mostrar las formas tridimensionales de las moléculas ó de iones
poliatómicos
EN LACES COVALENTES POLARES Y NO POLARES :
Los átomos similares
que comparten electrones poseen una distribución de cargas simétricas
permitiendo definir propiedades isotrópicas en las moléculas es decir no tiene
regiones preferenciales de electronegatividad como es el caso de los compuestos
de cloro y los de hidrógeno gaseoso.  este tipo de en lace se denomina no polar o
apolar en función de la diferencia de electronegatividades DE =
0.
este tipo de en lace se denomina no polar o
apolar en función de la diferencia de electronegatividades DE =
0.

Los enlaces donde el par de
electrones nose comparten por igual
dejando una región carga eléctricamente forman moléculas asimétricas , como es
el caso del cloruro de hidrógeno, estos modelos de densidad electrónica
permiten definir la polaridad de las moléculas 

 y predicen la
distribución de la nube de cargas electrónicas o dipolo
y predicen la
distribución de la nube de cargas electrónicas o dipolo 

 , la mínima densidad esta en el hidrógeno y la máxima en el
cloro y las distribuciones se realizan resolviendo la ecuación de
Schrödinger.
, la mínima densidad esta en el hidrógeno y la máxima en el
cloro y las distribuciones se realizan resolviendo la ecuación de
Schrödinger. 



Para el agua el modelo presentado a continuación de la
densidad electrónica en el agua , el oxigeno tiene gran densidad electrónica, y
los hidrógenos baja por lo tanto el oxigeno esta cargado  y los hidrógenos
tiene carga parcial
y los hidrógenos
tiene carga parcial  . La afinidad electrónica del oxigeno es de 141 jJ/mol y el
oxigeno solo 73 kJ/mol. La energía de ionización del O es de 1314 kJ/mol, mas o
menos la del hidrógeno qure es de 1312 kJ/mol.
. La afinidad electrónica del oxigeno es de 141 jJ/mol y el
oxigeno solo 73 kJ/mol. La energía de ionización del O es de 1314 kJ/mol, mas o
menos la del hidrógeno qure es de 1312 kJ/mol.

QUIMICA INORGANICA
Definición de Química Inorgánica
 La
química inorgánica es la rama de la química que estudia las
propiedades, estructura y reactividad de los compuestos inorgánicos.
La
química inorgánica es la rama de la química que estudia las
propiedades, estructura y reactividad de los compuestos inorgánicos. Este campo de la química abarca todos los compuestos químicos descontando los que tienen enlaces carbono-hidrógeno, que son objeto de estudio por parte de la química orgánica.
Ambas disciplinas comparten numerosos puntos en común, y están surgiendo campos interdisciplinares de gran importancia, entre los que podemos citar la química organometálica.
La parte más importante de los compuestos inorgánicos se forman por combinación de cationes y aniones unidos por enlaces iónicos. Así, el NaCl se forma por unión de cationes sodio con aniones cloruro. La facilidad con la que se forma un compuesto iónico depende del potencial de ionización (para el catión) y de la afinidad electrónica (para el anión) de los elementos que generan los iones respectivos.
Los compuestos inorgánicos mas importantes son los óxidos, carbonatos, sulfatos, ect. La mayor parte de los compuestos inorgánicos se caracterizan por puntos de fusión elevados, baja conductividad en estado sólido y una importante solubilidad en medio acuoso.
A nivel industrial, la química inorgánica, tiene una gran importancia. Se acostumbra a medir el desarrollo de una nación por su productividad en ácido sulfúrico. Entre los productos químicos más fabricados a nivel mundial cabe citar el sulfato amónico, amoniaco, nitrato amónico, sulfato amónico, ácido hipocloroso, peróxido de hidrógeno, ácido nítrico, nitrógeno, oxígeno, carbonato de sodio…….
ONDAS Y SONIDO
ONDAS Y SONIDO
Una
onda es una perturbación que avanza o que se propaga en un medio material o
incluso en el vacío. Cuando estas ondas necesitan de un medio material, se
llaman ondas mecánicas. Las únicas ondas que pueden propagarse en el
vacío son las ondas electromagnéticas.
El
sonido es un tipo de onda mecánica que se propaga únicamente en presencia de un
medio material.
Un cuerpo al
vibrar imprime un movimiento de vaivén (oscilación) a las moléculas de aire que
lo rodean, haciendo que la presión del aire se eleve y descienda
alternativamente. Estos cambios de presión se trasmiten por colisión entre las
moléculas de aire y la onda sonora es capaz de desplazarse hasta nuestros
oídos. Las partes de la onda en que la presión aumenta (las moléculas se juntan)
se llaman compresiones y aquellas en que la presión disminuye (las moléculas se
alejan) se llaman enrarecimientos.
Según la
dirección de propagación, clasificamos las ondas en dos tipos:
Ondas Longitudinales:
Es cuando la vibración
de la onda es paralela a la dirección de propagación de la propia onda. Estas
ondas se deben a las sucesivas compresiones y enrarecimientos del medio, de
este tipo son las ondas sonoras. Un resorte que se comprime y estira también da lugar a una
onda longitudinal.
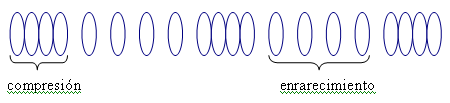 |
El sonido se trasmite en el aire
mediante ondas longitudinales.
Otro ejemplo de onda longitudinal es quella que se
produce cuando se deja caer una piedra en un estanque de agua, Se
origina una perturbacion que se propaga en circulos concéntricos que,
al cabo del tiempo, se extienden a todas las partes del estanque.
Ondas Transversales:
Donde la vibración es perpendicular a la dirección de la onda. Las ondas transversales se caracterizan por tener montes y valles. Por ejemplo, las ondas que se forman sobre la superficie del agua al arrojar una piedra o como en el caso de una onda que se propaga a lo largo de una cuerda tensa a la que se le sacude por uno de sus extremos.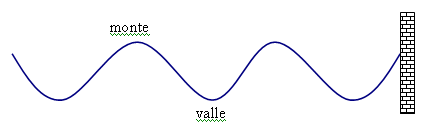 |
Características generales o elementos de las ondas
Tren de ondas: Todas las ondas al moverse lo hacen una tras otra como si fuera un tren de donde se coloca un vagon tras otro.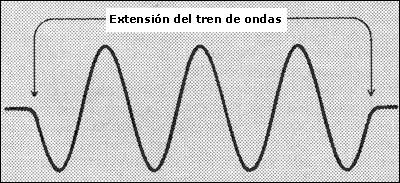 |
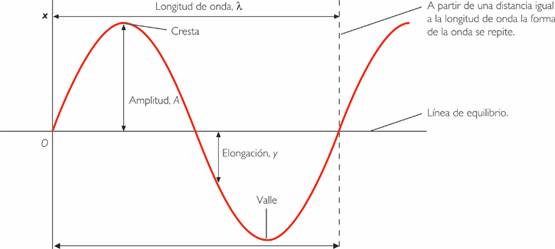
Nodo: Es el punto donde la onda cruza la línea de equilibrio.
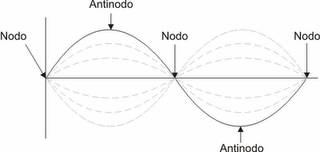 |
Elongación: Es la distancia entre cualquier punto de onda y su posición de equilibrio.
Cresta, monte o pico: es el punto más alto de una onda
Valle: Es el punto más bajo de una onda.
 |
Periodo: Tiempo que tarda en efectuarse una onda o vibracion completa, se mide en segundos o s/ciclo se representa con una T mayúscula.
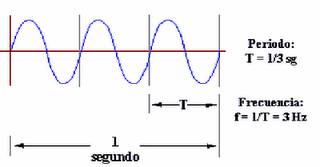 |
Notemos que el periodo (T) es igual al recíproco de la frecuencia (f) y viceversa.
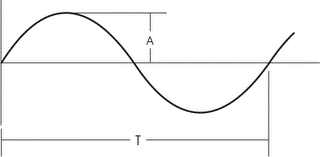
Amplitud (A) : Es la maxima separacion de la onda o vibración desde su punto de equilibrio.
 |
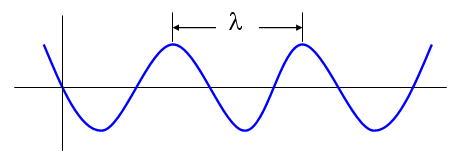
La longitud de onda (λ) es la distancia entre dos máximos o compresiones consecutivos de la onda. En las ondas transversales la longitud de onda corresponde a la distancia entre dos montes o valles, y en las ondas longitudinales a la distancia entre dos compresiones contiguas. También podemos decir que es la distancia que ocupa una onda completa, se indica con la letra griega lambda (Λ) y se mide en metros. A la parte superior de la onda se le llama cresta y a la inferior se le llama valle.
Tomaremos como ejemplo ilustrativo una onda transversal.
 |
Frecuencia: Es el número de ondas producidas por segundo. La frecuencia se indica con la letra f minúscula. Se mide en ciclos/ segundo o hertz (Hz). Coincide con el número de oscilaciones por segundo que realiza un punto al ser alcanzado por las ondas.
Las dos magnitudes anteriores, longitud y frecuencia, se relacionan entre sí para calcular la velocidad de propagación de una onda.
Velocidad de propagación: Es la relación que existe entre un espacio recorrido igual a una longitud de onda y el tiempo empleado en recorrerlo.
Se indica con la letra V y es igual al producto de la frecuencia (f) por la longitud de onda (λ).
Matemáticamente se expresa así:
por lo tanto
fórmula que nos indica que la longitud de onda λ y la frecuencia f son dos magnitudes inversamente proporcionales, es decir que cuanto mayor es una tanto menor es la otra.
Ver: PSU: Física;
Periodo: Es el tiempo (en segundos) que tarda un punto en realizar una oscilación completa al paso de una onda. Se abrevia con la letra (T).
La frecuencia (f) se relaciona con el periodo según la fórmula
Volvamos a la fórmula
para reemplazar en ella f (frecuencia), y nos queda la fórmula
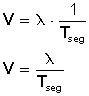
Lo cual nos indica que también podemos calcular la velocidad si conocemos la longitud (λ) y el periodo (en segundos) de una onda.
Como vemos, podemos relacionar estas magnitudes y conociendo los valores de algunas de ellas podemos determinar los valores de las otras, usando las fórmulas indicadas.
Suscribirse a:
Comentarios (Atom)



